上海交通大学Bio-X研究院李璨课题组与国家纳米科学中心丁宝全课题组通力合作,在物理和材料领域的顶级学术期刊《ACS applied materials & interfaces》于2017-2018连续发表两篇重要论文。上海交通大学曲艺姣硕士与杨娟娟博士分别为论文的第一作者。
DNA是生物体内的重要遗传物质,其序列碱基遵循碱基互补配对原则。正是由于DNA强大的可编程能力,研究人员可以通过理性设计获得任何想要的DNA序列。而正是基于沃森-克里克的碱基互补配对原则,DNA大分子能够在溶液中自组装形成多种多样的纳米结构。DNA纳米材料具备形貌可控性、可寻址性、可修饰性等优点,作为生物大分子,DNA具有其他材料不可比拟的生物安全性,这为DNA纳米材料作为药物载体提供了强有力的支持。
|
|
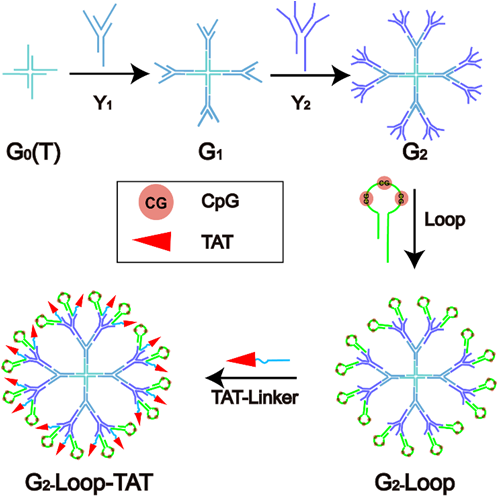
而在另一项合作课题中,DNA树枝状大分子被用作CpG免疫刺激剂的载体。连接了TAT穿膜肽的DNA树枝状大分子获得了更强的巨噬细胞内化。功能化的DNA树枝状大分子能够有效运输免疫刺激剂CpG并获得了理想的免疫刺激效果。
李璨团队近些年发表多篇相关论文,推动纳米技术在生物医药领域的应用。
文章信息:
1. Qu Y, Yang J, Zhan P, et al. Self-Assembled DNA Dendrimer Nanoparticle for Efficient Delivery of Immunostimulatory CpG Motifs.[J]. Acs Appl Mater Interfaces, 2017, 9(24):20324-20329.
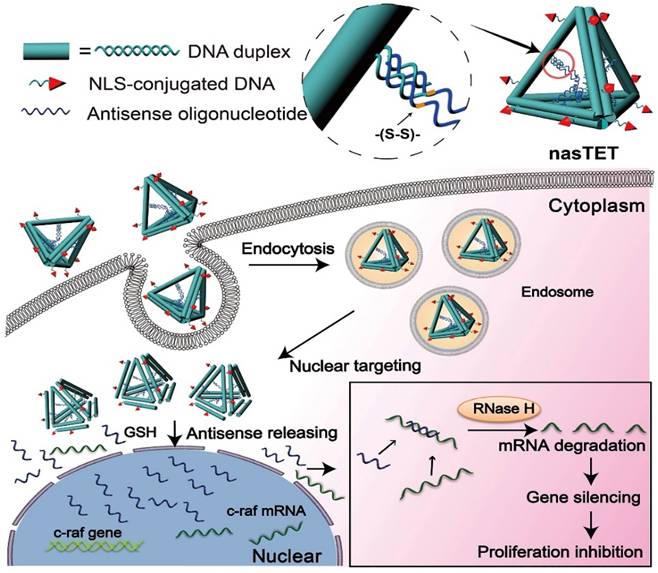
2. Yang J, Jiang Q, He L, et al. Self-assembled Double Bundle DNA Tetrahedron for Efficient Antisense Delivery[J]. Acs Applied Materials & Interfaces, 2018, 10(28).
论文链接:
1. https://pubs.acs.org/doi/10.1021/acsami.7b05890
2. https://pubs.acs.org/doi/10.1021/acsami.8b07889