2021年10月27日,上海交通大学Bio-X研究院吴际教授团队在著名学术期刊Biomaterials (IF 12.475)在线发表题为Generation ofoffspring-producing 3D ovarian organoids derived from female germline stem cellsand their application in toxicological detection的研究论文。该研究利用3D培养系统率先建立了由雌性生殖干细胞衍生的卵巢类器官系统,并利用该系统将雌性生殖干细胞体外高效分化至功能卵母细胞, 经体外受精后产生健康子代。上海交通大学Bio-X研究院吴际教授和深圳市儿童医院马廉教授为论文共同通讯作者,Bio-X研究院李小勇博士为论文第一作者。
生殖是一切生命体的基本特征之一,物种的延续必须依赖于生殖。生殖细胞为直接完成这一功能的细胞。生殖干细胞是生殖细胞的早期阶段,传统观念认为女性和绝大多数雌性哺乳动物出生后卵母细胞数目不再增加, 只会不断减少。2009 年吴际教授团队首次从新生和成年的小鼠卵巢内分离出雌性生殖干细胞并对其进行特征化 (NatureCell Biology), 从而发现成年哺乳动物卵巢内存在雌性生殖干细胞。随后, 吴际教授实验室及其他团队分别从大鼠、猪、羊、猴和人的卵巢内分离出雌性生殖干细胞及揭示其调控因子,并利用雌性生殖干细胞成功构建基因修饰动物模型。2017年,通过追踪移植的雌性生殖干细胞在小鼠卵巢内的发育,吴际教授团队揭示雌性生殖干细胞具有归巢特征及其发育规律,在体内分化为能产生健康后代的功能卵母细胞 (MolecularTherapy, IF 11.454)。然而,雌性生殖干细胞能否在体外发育为功能卵母细胞及其体外发育特征尚未见报道。
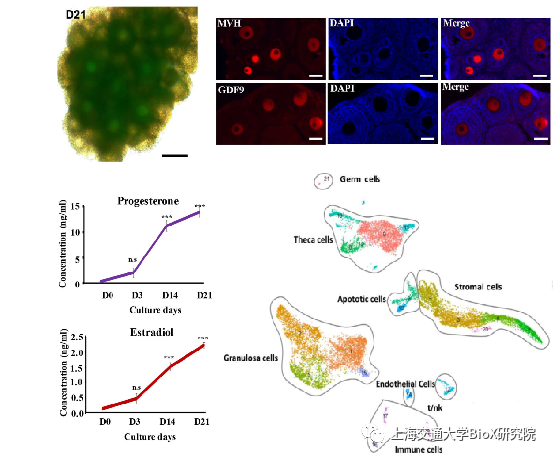
吴际教授团队利用3D培养系统建立了由小鼠雌性生殖干细胞衍生的卵巢类器官模型。卵巢类器官像正常的卵巢一样,充满卵泡并具有激素分泌功能。通过单细胞测序,吴际教授团队揭示卵巢类器官含有生殖细胞、颗粒细胞、卵泡膜细胞和成纤维细胞等7个细胞群 (图1)。从卵巢类器官中分离卵泡,经体外培养可发育至成熟卵母细胞。而成熟卵母细胞经体外受精可产生正常的后代。这些结果表明吴际教授团队成功建立了雌性生殖功能细胞体外高效分化至可产生后代的功能卵母细胞系统。为不孕不育及相关疾病诊治和生育力保存提供技术平台和理论依据,为雌性生殖干细胞的临床应用奠定基础。
此外,吴际教授团队最近还在国际学术期刊Journal of Advanced Research (IF 10.475)在线发表题为Offspring production ofovarian organoids derived from spermatogonial stem cells by defined factorswith chromatin reorganization的研究论文。通过探究精原干细胞命运调控机制,发现印记基因 (H19, Zfp57) 和转录因子(Stella和Plzf)在精原干细胞向雌性生殖细胞转换中起关键作用。并在此4个因子的诱导下,精原干细胞能转换为类雌性生殖干细胞的细胞。随后,利用卵巢类器官系统,成功的将精原干细胞诱导的类雌性生殖干细胞分化至卵母细胞,体外受精后,得到健康子代 (图2)。该成果为性决定与性分化相关疾病的诊治提供理论基础。上海交通大学Bio-X研究院吴际教授和系统生物医学研究院赵小东教授为论文共同通讯作者,吴际教授团队的罗华程、李小勇和Geng Tian为论文共同第一作者。
上述研究得到了国家自然科学基金国际合作重点项目、科技部重点研发计划等项目的支持。