2024年9月25日23时,上海交通大学Bio-X研究院马凯玥博士与美国耶鲁大学Monkol Lek团队合作,在Cell杂志在线发表了题为“Saturation Mutagenesis-Reinforced Functional Assays for Disease-related Genes”的研究文章。
研究人员建立了一种适用于研究疾病基因的深度突变筛选工作流程“饱和诱变助力的功能方法”——SMuRF 。该工作流程包含一种全新易操作且成本较低的饱和诱变方法、一种全新灵敏高通量的流式细胞仪功能方法以及多种独立验证性功能方法,可实现对多种疾病基因的快速高效深度突变筛选。
另外,为验证和展现SMuRF的有效性,研究人员应用SMuRF对两种α-抗肌萎缩相关糖蛋白病基因FKRP和LARGE1所有可能的单核苷酸突变进行了功能打分。结果显示,SMuRF的建立和应用为研究各种罕见病的功能突变提供了可能性。

致病遗传变异的解析一直是人类遗传学领域的一个重要挑战。孟德尔遗传病相关基因的单核苷酸突变本应是人类遗传学中最容易研究的突变类型,然而对于许多疾病基因来说,至少超过半数的单核苷酸突变的临床重要性尚未得到确定,严重影响了遗传疾病尤其是罕见遗传病的诊断效率。深度突变筛选(Deep mutational scanning, DMS)是指通过饱和诱变产生大规模的基因变异继而在细胞系中通过高通量方法研究遗传变异的研究方法,该方法可以极大加快遗传病诊断速度,深化我们对单核苷酸突变临床重要性的认识。然而,当前深度突变筛选方法的成本和复杂性皆阻碍了相关方法在临床研究中的广泛应用。
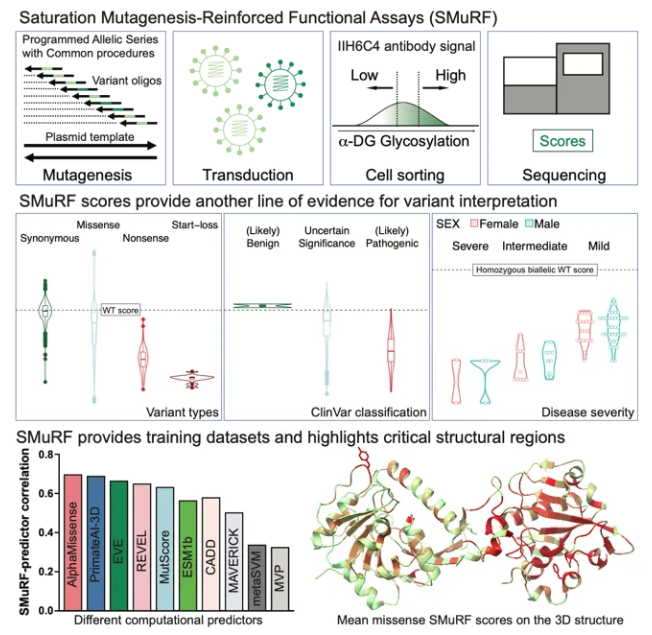
图一.SMuRF生物技术开发及应用示意图
饱和式基因组(碱基)编辑 (SGE/SBE)是当前最广泛使用的饱和诱变方法之一,但是其应用成本较高,且其受限于CRISPR系统的编辑效率差异,使得不同位点产生突变的覆盖程度存在难以预测的差异。因此,在临床研究中,SGE和SBE难以在缺乏CRISPR技术经验的疾病研究实验室中获得广泛应用。
与SGE/SBE不同,PALS(programmed allelic series)是一种可以无偏好产生高覆盖饱和式突变的方法(PMID: 25559584)。研究人员基于PALS开发了同样具有无偏好性、高覆盖性,且成本低廉、操作简单的PALS-C方法。此外,在分子生物学生物技术开发的基础上,研究人员专注于探究突变对细胞功能改变的影响,优化改良了一种流式细胞仪功能探测方法,高效提升了对DMS检测的灵敏度。
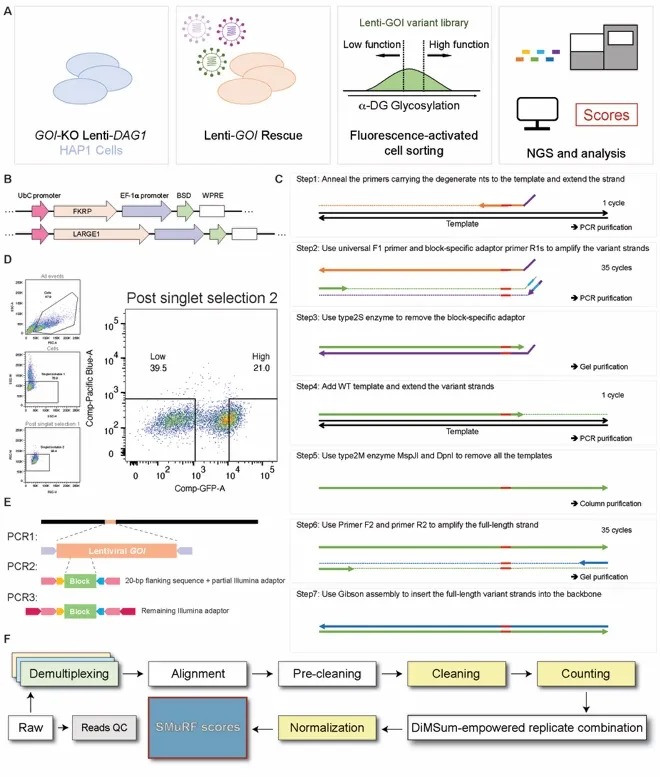
图二. SMuRF工作流程技术细节
同时,基于上述生物技术方法的开发优化,研究人员采用SMuRF对FKRP及LARGE1的遗传突变进行功能研究。FKRP和LARGE1均为参与α-DG糖基化的酶。FKRP的功能是将第二个Rbo5P添加到Rbo5P串联体中,而LARGE1则负责添加matriglycan的重复二糖单元。目前,针对与FKRP或LARGE1相关的α-抗肌萎缩相关糖蛋白病的新药、基因疗法和细胞疗法正在积极开发中。因此,增强对这两个基因突变的认识,可以协助患者参与到这些正在进行中的基因特异性试验。
与人类遗传变异数据库ClinVar及最大规模人类遗传变异体数据库gnomAD进行比较后,研究人员确认SMuRF打分与数据库中报道的变异临床分类和变异频率相符合。接着,研究人员通过整合8个患者队列发现SMuRF打分可以较好地反映FKRP相关疾病的严重程度。研究人员还比较了SMuRF和以AlphaMissense为代表的(人工智能)变异预测工具的功能打分,提出SMuRF有希望进一步提升相关人工智能工具的预测能力。随后,研究人员将SMuRF打分投射到了FKRP和LARGE1的蛋白结构上,揭示了疾病相关的重要区域。最后,秉持着“独立的验证实验应是深度突变筛选工作流程中的重要一环”这一原则,研究人员使用基于LASV病毒入侵机制的高通量方法及免疫荧光染色验证方法在肌肉细胞系中对α-DG糖基化和SMuRF打分进行了验证。
本文所描述的SMuRF方法可以很容易地应用于其他至少12种α-抗肌萎缩相关糖蛋白病酶基因,且相关工作流程可以灵活地应用于其他罕见病基因的研究中。
综上,SMuRF提供了一种操作简便且具有成本效益的饱和诱变方法,其与高通量功能筛选技术相结合,能够有效解析临床上意义尚不明确的变异。SMuRF在预测疾病严重程度、解析关键结构区域,以及为计算预测模型提供训练数据集方面展现出广泛应用的潜力。
上海交通大学Bio-X研究院马凯玥博士(前耶鲁大学博士生)和耶鲁大学Monkol Lek教授为论文共同通讯作者。马凯玥博士为该文唯一第一作者。相关工作得到美国国立卫生研究院、美国肌营养不良症协会、陈·扎克伯格倡议和上海交通大学等支持。
目前,马凯玥博士与上海交通大学毛亚飞课题组合作,专注于第三代测序技术的临床应用及遗传疾病的生物学机制研究,课题组长期招聘博士后。Monkol Lek实验室专注于罕见遗传病的诊疗技术的开发,现招聘博士后研究人员及学士后研究助理。欢迎有志于深入探索相关领域的同行联系。
文章链接:https://doi.org/10.1016/j.cell.2024.08.047